体外诊断试剂生产管理要求与风险控制水平相关。监管部门对于不同类型体外诊断试剂产品有不同的法规要求。在我国,大部分体外诊断试剂属于医疗器械管理,生产过程需要符合《体外诊断试剂生产和质量管理规范》的要求,但用于血源筛查的体外诊断试剂属于药品管理,其生产过程需要符合GMP的要求
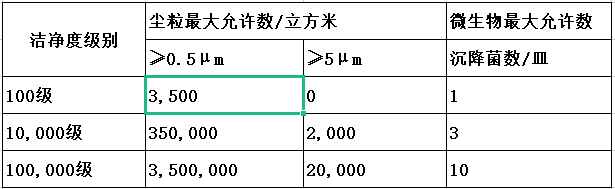
条对生产环境有净化要求的产品除应当满足《体外诊断试剂生产实施细则》的通用要求外,其生产环境还应当满足本附录的要求。不同洁净级别生产区域的控制标准参见下表:
不同洁净级别生产区域的控制标准文库
第二条企业应当明确工艺所需的空气净化级别,进入洁净室(区)的空气必须净化。阴性、阳性血清、质粒或血液制品的处理操作应当在至少10,000级环境下进行,与相邻区域保持相对负压,并符合防护规定。酶联免疫吸附试验试剂、免疫荧光试剂、免疫发光试剂、聚合酶链反应(PCR)试剂、金标试剂、干化学法试剂、细胞培养基、校准品与质控品、酶类、抗原、抗体和其他活性类组分的配制及分装等产品的配液、包被、分装、点膜、干燥、切割、贴膜、以及内包装等工艺环节,至少应在100,000级净化环境中进行操作。无菌物料的分装必须在局部百级。普通化学类诊断试剂的生产应在清洁环境(符合本细则第二十条规定)中进行。
第三条厂房应当具有防止昆虫和其他动物进入的设施。
第四条企业应当提供洁净区内生产工艺流程图和空气调节、配电照明等平/立面图。新建、改建、扩建的洁净区厂房应当提供有资质的设计单位设计的图纸。
第五条在设计和建设厂房时,应当考虑使用时便于进行清洁工作。洁净室(区)的内表面应平整光滑、无裂缝、接口严密、无颗粒物脱落,并能耐受清洗和消毒,墙壁与地面的交界处宜成弧形或采取其他措施,以减少灰尘积聚和便于清洁。
第六条洁净区应当配置空气消毒装置,有平面布置图、编号和使用记录。
第七条洁净室(区)内各种管道、灯具、风口以及其他公用设施,在设计和安装时应考虑使用中避免出现不易清洁的部位。
第八条洁净室(区)应当根据生产要求提供足够的照明。主要工作室的照度宜为300勒克斯;对照度有特殊要求的生产部位可设置局部照明。厂房应当具有应急照明设施。
第九条洁净室(区)的窗户、天棚及进入室内的管道、风口、灯具与墙壁或天棚的连接部位均应密封。
第十条更衣室、浴室及厕所的设置不应对洁净室(区)产生不良影响。




